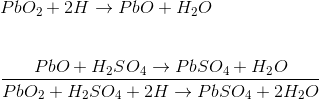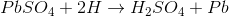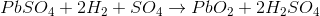铅酸电池的工作
存储电池或二次电池是这样的电池,其中电能可以作为化学能量存储,然后将这种化学能转换成电能,如所需。通过施加外部电源将电能转化为化学能量作为电池的充电。尽管将化学能转换成用于供应外部载荷的电能被称为二次电池的放电。
中电池充电那当前的通过它,引起电池内的一些化学变化。这种化学改变在形成期间吸收能量。
当电池连接到外部负载时,化学变化以相反的方向进行,在此期间吸收的能量被释放为电能并提供给负载。
现在我们将尝试了解原则铅酸电池的工作为此,我们将首先讨论铅酸蓄电池这通常用作蓄电池或二次电池。
用于铅酸蓄电池电池的材料
构建铅酸电池所需的主要活性材料是
- 过氧化铅(PBO2)。
- 海绵铅(PB)
- 稀硫酸(h2所以4.)。
过氧化铅(PBO2)
正板由过氧化铅制成。这是深棕色,硬质和脆性的物质。
海绵铅(Pb)
负极板由纯海绵状况的纯铅制成。
稀硫酸(h2所以4.)
用于稀硫酸铅酸蓄电池具有水的比例:酸= 3:1。
这铅酸蓄电池通过浸入过氧化物板和稀硫酸中的海绵铅板形成。负载在这些板之间外部连接。在稀硫酸中,酸分子分成正氢离子(H.+)和阴性硫酸盐离子(所以4.- -)。在PbO到达时氢离子2板,它们从中接收电子并成为氢气原子再次攻击PBO2并形成pbo和h2o(水)。这种PBO与H反应2所以4.并形成PBSO4.和H.2o(水)。
所以4.- -离子在解决方案中自由移动,因此它们中的一些将达到纯PB板,在那里它们给出额外的电子并成为激进的4.。作为激进的所以4.不能单独存在它将攻击PB并将形成PBSO4.。
作为h.+离子从pbo取电子2板材等等4.- -离子给PB板电子给PB板,在这两个板之间存在电子的不等式。因此,通过这些板之间的外部负载将存在电流的流动,以平衡电子的不等式。该过程称为铅酸电池的放电。
硫酸铅(PBO4.)颜色发白。在卸货期间,
- 两块板都覆盖了PBSO4.。
- 由于PBO反应过程中的水形成,硫酸溶液的比重下降2盘子。
- 结果,反应率落下,意味着潜在差异在放电过程中板之间减少。
现在我们将断开负载并连接PBSO4.覆盖着PBO.2板与外部直流源和PBO的正末端2覆盖有PB板,具有该直流源的负端子。在放电期间,硫酸的密度落下,但溶液中存在仍然存在硫酸。该硫酸也仍然是h+所以4.- -在溶液中的离子。氢离子(阳离子)正充电,移动到与DC源的负端连接的电极(阴极)。这里每个H.+离子从中取一个电子并变成氢原子。然后这些氢原子攻击PBSO4.并形成铅和硫酸。
所以4.- -离子(阴离子)朝向与DC源的正极连接的电极(阳极)移动,在那里它们会放弃额外的电子并成为激进的4.。这个激进的所以4.不能单独存在,因此与PBSO反应4.阳极和形成铅过氧化物(PbO2)和硫酸(h2所以4.)。
因此,通过对铅酸蓄电池进行充电,
- 铅硫酸铅阳极转化为过氧化铅。
- 阴极的铅硫酸盐转化为纯铅。
- 终端;细胞的潜力增加。
- 硫酸的比重增加。